铂类药物是目前临床常见广谱抗肿瘤药物,已深度整合入结直肠癌、卵巢癌、肺癌等实体瘤的标准化治疗体系,成为多种恶性肿瘤一线及联合方案的核心组分。然而,铂类药物的副作用显著 (如神经毒性、肾毒性、耳毒性等),因此实时监测血液中具有药理活性的“超滤铂”浓度对于优化疗效与个性化化疗方案的制定至关重要。目前,在临床实践中,铂类药物的药代动力学监测几乎处于空白状态。传统的分析方法虽然可以检测总铂浓度,无法直接进行“超滤铂”浓度检测,另外存在存在检测流程复杂、设备庞大、灵敏度不足,药代动力学参数与组学数据割裂等问题。
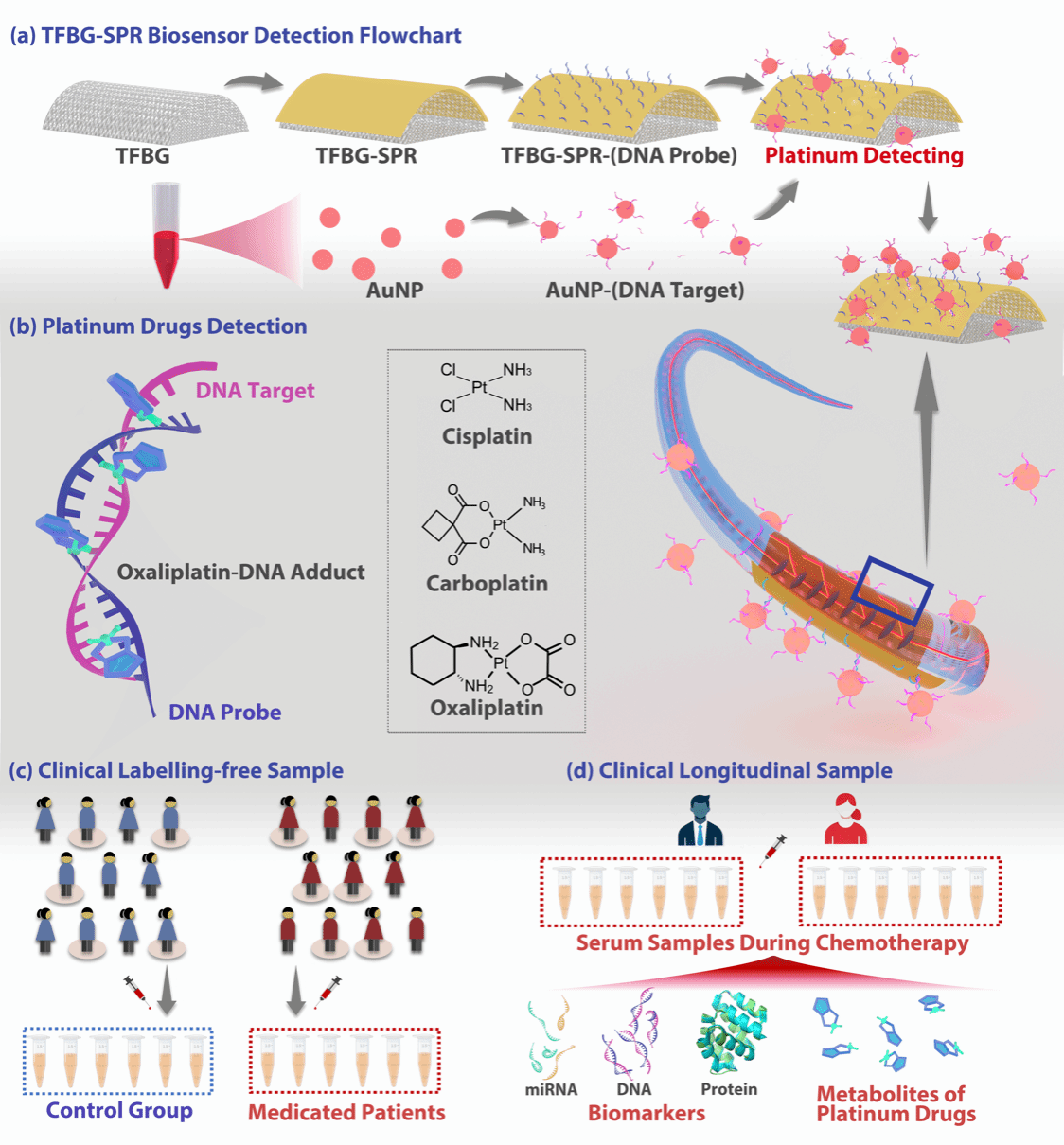
大连理工大学物理学院先进光学与光纤传感彭伟教授课题组与大连理工大学附属肿瘤医院(辽宁省肿瘤医院)检测科、神经外科、妇科展开深度合作,以倾斜光纤布拉格光栅表面等离子共振 (TFBG -SPR) 技术的光纤传感元件为核心,结合DNA靶向捕获探针,实现了临床铂类化疗物的高特异性、超痕量POCT检测,为化疗过程中铂药的药代动力学分析提供了有效方案;另外同步开展癌症标志性核酸序列miRNA-21的多组学分析,最终服务于精准化疗的、管理与个体化治疗决策提供动态数据,并首次通过POCT临床快检平台技术发现了铂药和miRNA在预后化疗周期的负相关性。该成果以“Plasmonic Fiber Optic Sensing Platform for Point-of-Care Pharmacokinetic Monitoring of Platinum Chemotherapeutics: Toward Ultra-trace Multi-Omics Precision Chemotherapy Management”为题发表于ACS Sensors,第一作者为大连理工大学物理学院博士研究生段怡凡,通讯作者为大连理工大学物理学院张扬副教授、辽宁省肿瘤医院检测科主任郑阳医生以及结直肠科李永民医生。
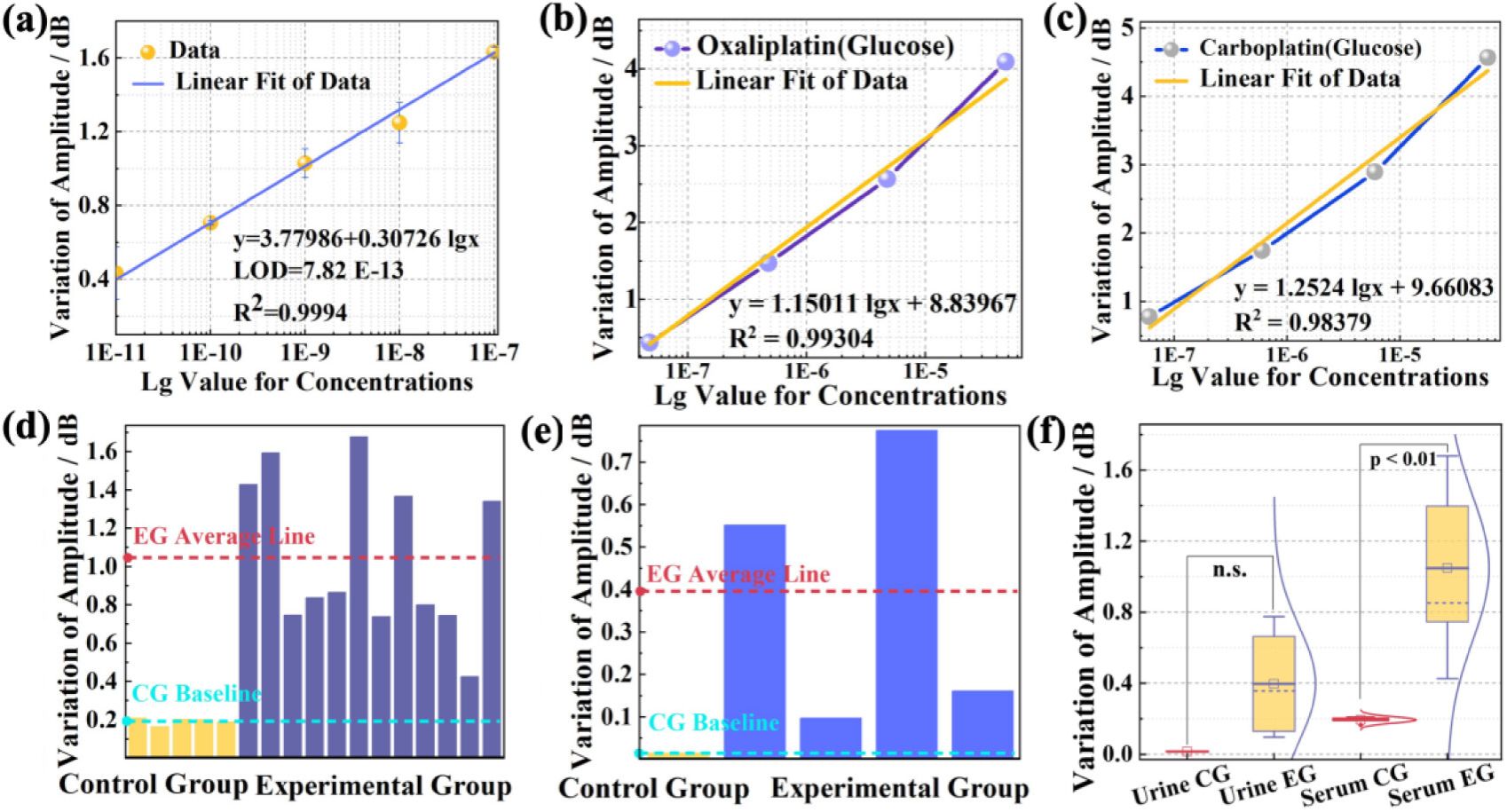
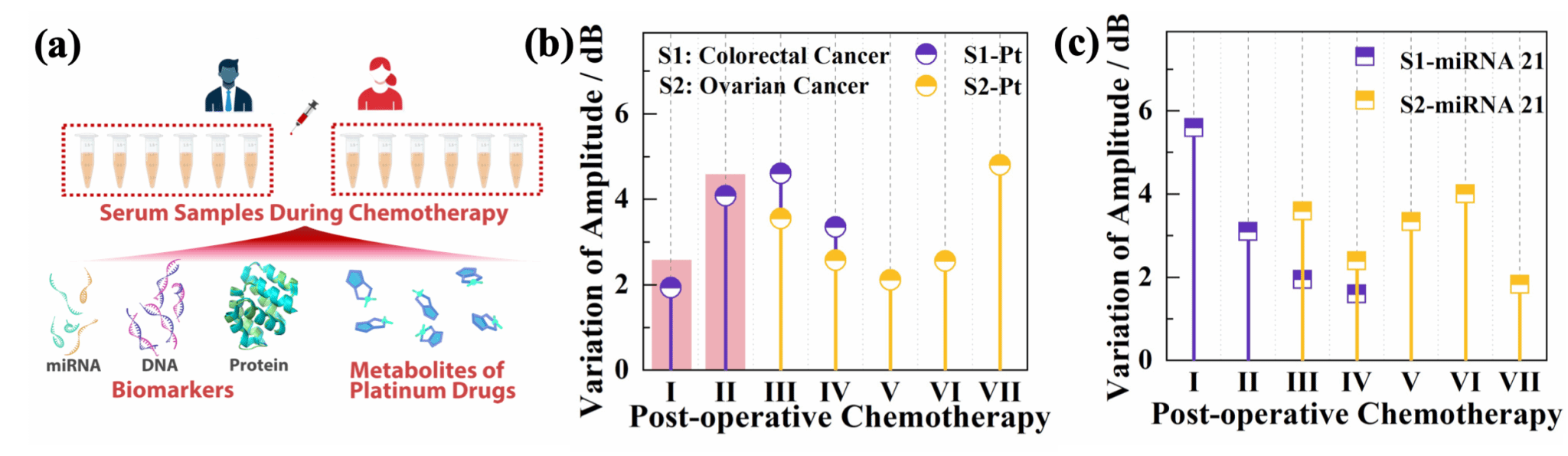
该平台的检测范围在10 pM至0.1 μM之间,检出限为782 fM,且覆盖临床有效浓度区间,对Pb2+、Mn2+、Cu2+、Ca2+等常见金属离子无交叉响应,检测结果有较高的可重复性,三次独立实验标准差小于5%,检测结果具备良好的可靠性。在临床样本中,对30例临床血清与尿液免标记样本进行检测,用药组与健康对照组信号差异显著 (P < 0.01)。另外,得益于DNA靶向识别探针的灵活可编程性,通过改变探针序列,可以将该检测方案拓展至miRNA、ctDNA、标志性蛋白等重要临床生物标志物的检测应用中。检测方案具备高度通用性与可编程性,为多癌种、多标志物联合监测提供技术基础。并通过深入开展临床横向免标记与纵向队列样本综合检测研究,采集结直肠癌与卵巢癌患者化疗前后血清样本,进行无标签、超痕量快检,揭示了铂药浓度与miRNA-21表达水平之间的潜在负相关关系,验证了平台临床适用性与生物标志物潜力。该工作结合学校医工交叉合作的契机,通过光纤智能感知技术团队和肿瘤临床医生团队多年合作,为精准化疗的动态监测与个体化剂量调整提供了标准化、集成化、智能化的技术方案,为后期AI整合数据以实现多组学辅助诊疗模型的搭建提供了有效的解决途径,具备潜在的临床转化前景。
ACS Sensors 2025 10 (8), 6010-6019/DOI: 10.1021/acssensors.5c01492
